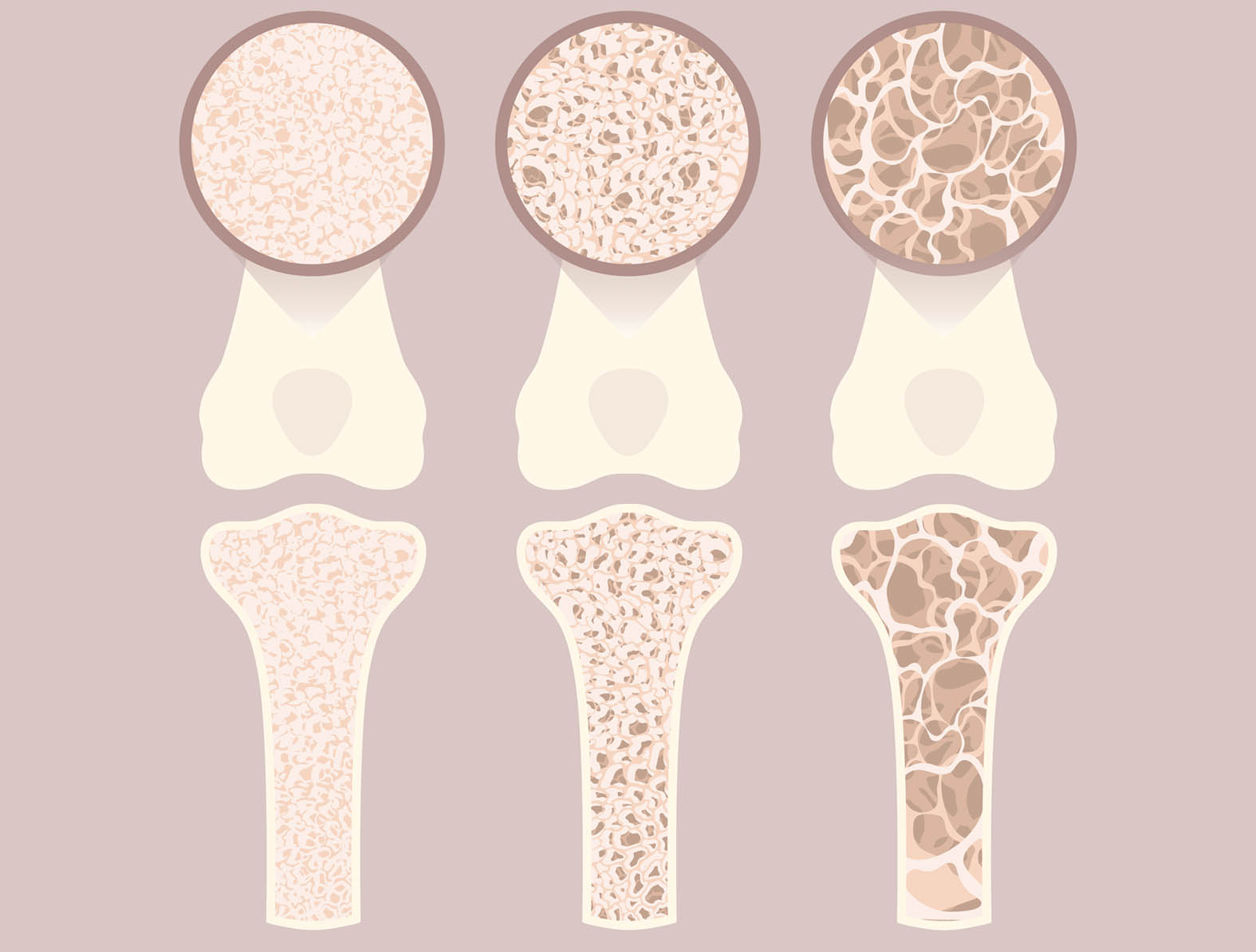
Implantate, die sich in nichts auflösen
Gute Ideen sind einfach: An Stelle von Implantaten aus Metall verwenden Chirurgen Stifte, Schrauben und Knochenersatzmaterialien aus Kunststoff. Diese baut der Körper selbstständig ab, so dass einige Monate nach Verheilung des Bruches auch vom Implantat nichts mehr zu sehen ist.
So weit die Theorie. In der Praxis können Probleme auftreten: Der Körper reagiert auf den Kunststoff stärker als auf ein Titan- oder Stahlimplantat. Die Abbauprodukte können, wenn diese in großen Mengen während eines kurzen Zeitraums auftreten, die gesunde Knochensubstanz angreifen.
Dennoch: Können die Komplikationen bezwungen werden, werden Kunststoffe im Operationssaal bald häufiger zu sehen sein als bisher – neben dem Routineeinsatz als Kordel oder OP-Naht auch häufiger als Stift und Schraube oder sogar als Knochenersatzmaterial.
Schon vor 30 Jahren setzten Operateure erstmals Kordeln und Operationsnähte ein, die im Inneren des Körpers nach dem Vernähen eines Schnitts zurückblieben und nach einigen Wochen auf keinem Röntgenbild mehr zu sehen waren. Das Material: Der Kunststoff Polydioxanon, ein zugkräftiger Kunststoff, der nach einigen Wochen, wenn die Wunde schon gut verheilt ist, an Festigkeit verliert und von den Fresszellen des Menschen vollständig entfernt wird.
„Nach sechs Wochen haben Kordeln noch eine Reißkraft von etwa 50 Prozent, die danach kontinuierlich weiter abnimmt“, sagt Klaus E. Rehm von der Klinik und Poliklinik für Unfall-, Hand- und Wiederherstellungschirurgie der Universität Köln. „Gleichzeitig nimmt die Festigkeit im ehemals geschädigten Gewebe zu. Nachdem die Kordel nicht mehr zu sehen ist, ist auch die Wunde in der Regel vollständig verheilt.“
Ist beispielsweise eine Sehne verletzt, kann sie mit einer Kordel zusammengenäht werden. Sind die Außenbänder am Fuß gerissen, können künstliche Bänder, die parallel zu den verletzten Bändern genäht werden, dem Fußgelenk übergangsweise Halt geben. Bei einem Trümmerbruch der Kniescheibe legen Operateure „Rahmennähte“ an, um die Kraft besser zu verteilen.
„Sehnen und Bänder nehmen Zugkräfte auf“, erläutert Rehm, „dafür sind unsere Kunststoffbänder ideal geeignet“. Die Ärzte ersetzen natürliche Bänder also durch ein Imitat aus Kunststoff, ohne dass der Körper das merkt: Das Kunststoffband nimmt nun die Kraft auf, die sonst das Originalband zu tragen hätte. Der Vorteil hier: Infektionen oder Entzündungen rings um den Kunststoff sind selten, da die Fäden kaum einen Millimeter dick sind. Sie sind „bioresorbierbar“. „Der Körper integriert diese meist aus Polyester bestehenden Kunststoffe oder baut sie innerhalb kurzer Zeit ab“, erläutert Klaus E. Rehm, „entsprechend der Kunststoffzusammensetzung kann es auch bis zu fünf Jahren dauern. Zu schnelle, aber auch zu langsame Abbauprozesse können unerwünschte Reaktionen des umgebenden Gewebes hervorrufen“.
Auch als Nägel oder Schrauben
Chirurgen setzen „Nägel“ und „Schrauben“ vorwiegend ein, um kleine Knochen am Finger, an der Speiche, am Handgelenk und manchmal auch am Sprunggelenk mit bioresorbierbaren Implantaten aus Polylactid und Polyglycolid zu fixieren. „Bei herkömmlichen Polyglycolid-Stiften löst sich ein Teil der umgebenden Knochensubstanz bei mindestens jedem zweiten Patienten unbeabsichtigt auf“, sagt der Kliniker Rehm. Daher entwickelte er in Zusammenarbeit mit dem Ingenieur Lutz Claes aus dem Ulmer Kompetenzzentrum für Biomaterialien und mit der Firma BIOVISION GmbH den Polypin, einen Stift aus einem Polylactid-Co-Polymer. Dieses Polymermaterial wird gegenüber dem Polyglycolid deutlich langsamer abgebaut. Damit kann das umgebende Gewebe die Abbauprodukte ohne Nebenwirkungen beseitigen. Der Abbauprozess im Körper und die Reaktionen sind abhängig von der Größe des Implantates, der Fähigkeit des umgebenden Gewebes, die Abbauprodukte zu beseitigen, und von der Abbaugeschwindigkeit des Polymers, welche wiederum von der Zusammensetzung des Polymers beeinflusst wird. So arbeiten Prof. Rehm, Prof. Claes und die Firma BIOVISION an einer neuen Generation des Polypins. Bei diesem neuen Pin werden die Abbauprodukte des Polylactides, die Milchsäure, durch Zusätze von Tricalciumphosphat gepuffert und wird das Risiko der Auflösung der Knochensubstanz verringert. Allerdings verlängert sich durch den Zusatz der Abbauprozess des neuen Pins.
Matthias Epples Forschung zielt in eine ähnliche Richtung: Er erforscht Ersatzmaterialien für Knochen, die die umgebenden Gewebe möglichst gut vertragen und die ebenfalls keine sauren Abbauprodukte hervorbringen. Sein Basiskunststoff: Polyglycolid.
Um einen ausgeglichenen Säurewert, einen neutralen PH-Wert, zu bekommen, mischt auch der Wissenschaftler aus dem Institut für Organische und Anorganische Chemie an der Universität Hamburg das basisch wirkende Calciumphosphat zu dem Polyglycolid. Calciumphosphat – der Stoff, aus dem auch die Knochen sind – „puffert“ den Säureanteil ab, der durch den Abbau von Polyglycolid entsteht.
Allerdings testet Epple, den die Deutsche Forschungsgesellschaft (DFG) im letzten Jahr für seine Erforschung von neuen Biomaterialien mit dem Heinz Maier-Leibnitz-Preis auszeichnete, seine neue Idee noch im Labor, bevor er sein poröses Polymer mit Calciumphosphat bestückt. „Die Knochenauflösung kann damit vermutlich stark gebremst werden“, so Epple.
In der klinischen Praxis werden Knochenersatzmaterialien aus Polymeren noch nicht eingesetzt, aber Implantate aus Polymeren finden zahlreich Anwendung. „Knochen- oder Knorpelstücke, die sich vom Fingerknochen oder der knorpeligen Meniskusscheibe im Knie gelöst haben, können mit dem Polypin neu angeheftet werden“, sagt Klaus E. Rehm. Nach etwa zwei Jahren ist der Polypin auf einer Röntgenaufnahme nicht mehr zu sehen. Den Polypin gibt es in drei Größen mit einem Durchmesser von 1,5 mm, 2,0 mm und 2,7 mm. „Dickere Stifte machen keinen Sinn mehr“, sagt Rehm, „zum einen kann der Körper sie nur noch schwer abbauen, zum anderen sollten Kunststoffe nur bei nicht belasteten Knochenbrüchen verwendet werden“. Nach einem heftigen Unfall mit schweren Knochenbrüchen verwenden die Chirurgen der Kölner Uniklinik manchmal Titanschrauben mit einem Durchmesser von 4,5 Millimetern und noch dazu eine Titan-Platte. Diese Kräfte, die hier auf ein Implantat einwirken, hält kein Kunststoff aus.
Von sich aus bioresorbierbar sind Knochenstrukturen, die aus dem eigenen Körper stammen. So ersetzen Chirurgen, die beispielsweise nach einer schweren Beinverletzung mehrere Splitter eines Röhrenknochens entfernen mussten, verloren gegangene Knochen durch Knochen, den sie in einer vorhergehenden Operation aus dem Beckenkamm des Patienten herausschneiden. „Das ist zwar eine sichere Methode, doch manchmal reicht das Knochenmaterial nicht für den Defekt aus“, sagt Epple. Außerdem ist eine zusätzliche Operation nötig, in der Knochensubstanz dem eigenen „Reservoir“ entnommen wird.
„Besser wäre, wenn man künstliche Knochensubstanz hätte, mit der man die Defekte beheben kann“, sagt Epple, der mit seinem Konzept eines porösen Polyesters in einigen Jahren eine Alternative zu den bisherigen Knochenersatzstoffen bieten möchte.
Durch die Einlagerung von Salzkristallen in das Polyester, die nach dessen Synthetisierung herausgewaschen werden, wird die Oberfläche und damit die Kontaktfläche zu Knochenzellen sehr groß. Knochen bildende Zellen besiedeln diese Strukturen und durchwachsen die pergamentdünnen Wände, die sie viel leichter abbauen können als beispielsweise einen Stift von einigen Millimetern Stärke. Allerdings sind die Versuche Epples noch im In-vitro-Stadium. Mit der Besiedlung seiner Polyester hat der Chemiker erst vor einigen Wochen begonnen.
Bislang nutzt man die Knochensubstanz des Rindes. Aus diesem Knochen wird der organische Anteil durch spezielle chemische Verfahren entfernt. Sämtliche Proteine werden abgetötet und es bleibt damit „nur“ noch die Bälkchenstruktur des aus Calciumphosphat bestehenden Knochens übrig – der anorganische Anteil.
Die Bälkchenstruktur des Knochens wird zwar in der Regel ohne Probleme vom Körper akzeptiert, doch baut sich die neue Knochenstruktur um die des Rindes herum. Die Struktur der Rindersubstanz bleibt mindestens fünf Jahre erhalten – bioresorbierbar ist der so genannte „Endobone“ damit nicht. Allerdings ist dies auch nicht unbedingt nötig, da dem neuen Stück Knochen chemisch die gleiche Formel zu Grunde liegt.
Als Knochenersatzmaterialien gibt es neben Materialien von Rindern auch synthetische Materialien, z.B. Biobase (Sulzer Orthopedics). Biobase ist ein reines a-Tricalciumphosphat, das ebenfalls im Körper bzw. im Knochen abgebaut und durch neuen Knochen ersetzt wird.
„Der Bedarf an Knochenersatzmaterialien wird immer größer“, beteuert Matthias Epple, „die Menschen werden immer älter und die eigene Knochensubstanz immer schwächer“. Durch einen geeigneten Knochenersatzstoff könnte man hier akute Defizite ausgleichen – möglicherweise bald durch Kunststoffe, die der Körper erst akzeptiert und dann selbstständig abbaut. „Hier schlummert ein Milliardenmarkt“, meint Epple, der mit seinem Produkt, das bereits zum Patent angemeldet ist, in einigen Jahren Pharmariesen wie Merck oder Depuy-Johnson & Johnson das Wasser reichen will.
Ein Archivbeitrag* aus ORTHOpress 1 | 2000
*Archivbeiträge spiegeln den Stand zur Zeit der Erstveröffentlichung wieder. Die aktuelle Einschätzung des Sachverhalts kann durch Erfahrungszuwachs, allgemeinen Fortschritt und zwischenzeitlich gewonnene Erkenntnisse abweichen.